Fundamentos neurobiológicos
 |
FUNDAMENTOS NEUROBIOLÓGICOS DEL DOLOR EN EL MIEMBRO FANTASMA
Dr. PEDRO MONTOYA
UNIVERSIDAD DE LAS ISLAS BALEARES
RESUMEN
Se revisa la hipótesis de que un aumento de la excitabilidad del sistema nervioso central pudiera ser responsable del dolor en el miembro fantasma. Tras una breve descripción de los factores periféricos y centrales asociados a diversos fenómenos del miembro fantasma, se presenta evidencia procedente de estudios con técnicas no invasivas de neuroimagen de que en pacientes amputados se produce una reorganización funcional de la corteza somatosensorial. En concreto, estos estudios han demostrado que la organización del homúnculo en la corteza somatosensorial en pacientes con dolor fantasma es diferente a la de los pacientes sin dolor. Además, se ha encontrado una estrecha correlación entre la intensidad del dolor fantasma y el desplazamiento de la representación cortical del labio hacia la representación del miembro previa a la amputación. Estos resultados sugieren la existencia de una relación causal entre ambos fenomenos. Igualmente se ha sugerido que un aumento de la sensibilidad de las fibras A-beta podría constituir el mecanismo fisiológico que produce hiperexcitabilidad y plasticidad cortical asociada con el dolor en el miembro fantasma. Finalmente, se subrayan las implicaciones y la relevancia de estos datos para el desarrollo de terapias efectivas y la prevención del dolor en el miembro fantasma.
I. INTRODUCCIÓN
La aparición del miembro fantasma constituye la consecuencia más impresionante a la que se enfrentan los pacientes que sufren una amputación. Aunque en términos generales, este fenómeno hace referencia a la percepción real y viva del miembro amputado que se experimenta después de la amputación de una extremidad, el concepto fantasma puede ser empleado para la percepción de cualquier otra parte corporal amputada. La fuerte intensidad y la detallada descripción de las sensaciones fantasmas que hacen los pacientes afectados, sugiere que deben existir ciertos mecanismos fisiológicos que constituyan la base neurobiológica del miembro fantasma. A pesar de que la primera descripción científica del miembro fantasma data del siglo XVI (1), hasta la fecha sólo existen numerosos informes sobre su incidencia y sus características clínicas (Carlen et al, 1978;
Jensen et al, 1985; Sherman et al, 1984). Sin embargo, son escasas tanto las investigaciones sobre las causas y los mecanismos responsables del origen y el mantenimiento, como las terapias eficaces para la reducción del dolor en el miembro fantasma (Sherman, 1997).
Según la Asociación Internacional para el Estudio del Dolor (IASP) se ha de distinguir entre sensaciones dolorosas y no dolorosas en el miembro fantasma y en el muñón. De acuerdo con diversos estudios (Carlen et al, 1978; Jensen et al, 1985; Sherman y Sherman, 1983; Sherman et al, 1984), entre el 70 % y el 100 % de los pacientes amputados afirman experimentar con nitidez sensaciones exteroceptivas no dolorosas (por ejemplo, picor, la forma y movimiento de los dedos, etc.) procedentes del miembro fantasma. También se producen cambios en la longitud, el tamaño, la temperatura el volumen o la posición del miembro fantasma. Además, para el 60-85% de estos pacientes estas sensaciones son dolorosas. Los adjetivos usados para describir este dolor suelen ser los siguientes: sensación exagerada de hormigueo, picazón, ardor, presión, calambres, prurito, entumecimiento.
Los modelos explicativos existentes sobre la etiología del dolor en el miembro fantasma se fundamentan básicamente en mecanismos psicológicos o neurofisiológicos. Los modelos psicológicos subrayan el papel de factores cognitivos (atención) y emocionales (estrés, depresión, ansiedad, etc.). En general, hoy se puede afirmar que aunque la importancia de los factores psicológicos es evidente en el mantenimiento y reforzamiento del dolor, las causas de éste son fundamentalmente de carácter fisiológico. Entre los modelos neurofisiológicos se discuten mecanismos periféricos y centrales para explicar el dolor en el miembro fantasma.
En la primera parte de la presente revisión se expondrán los factores fisiológicos más discutidos en la literatura sobre el miembro fantasma. La segunda parte se dedicará a presentar evidencia experimental que apoya la existencia de cambios plásticos en pacientes con dolor en el miembro fantasma y exponer los mecanismos fisiológicos responsables. En la última parte se discutirán las implicaciones que tienen estos resultados para el desarrollo de terapias efectivas contra el dolor de los pacientes amputados.
II. FACTORES PERIFÉRICOS Y CENTRALES RELACIONADOS CON LA PERCEPCIÓN DOLOROSA DEL MIEMBRO FANTASMA
Existe una serie de observaciones clínicas y datos experimentales que apoyan la hipótesis de una causa fisiológica periférica para el dolor del miembro fantasma. Así se ha observado, por ejemplo: 1) que los dolores en el miembro fantasma están frecuentemente asociados a dolores en el muñón, 2) que en la zona inervada por el nervio lesionado se registra actividad neuronal espontánea, 3) que la estimulación sobre el muñón desencadena frecuentemente sensaciones en el miembro fantasma, y 4) que los dolores del miembro fantasma pueden ser reducidos a través de una anestesia local del muñón. Asimismo, numerosos estudios experimentales subrayan la importancia de mecanismos periféricos en la modulacion y mantenimiento del dolor del miembro fantasma. Algunas investigaciones han demostrado que el bloqueo del sistema nervioso simpático a través de fármacos (Marsland et al, 1982) o por medio de intervención quirúrgica (Kallio, 1950) produce una reducción significativa del dolor en pacientes amputados. Sin embargo, no existen muchas investigaciones que examinen sistemáticamente la relación entre la actividad nerviosa simpática y el dolor del miembro fantasma. Sherman et al (1989) encontró que pacientes que describían el dolor como una sensación de ardor mostraban una reducción del riego sanguíneo en el muñón, mientras que pacientes que sufrían de calambres presentaban característicos patrones de activación muscular en el muñón. Katz (1992) examinó diversas medidas psicofisiológicas de la actividad nerviosa simpática en tres grupos de amputados: pacientes con dolor del miembro fantasma, pacientes con sensaciones no dolorosas del miembro fantasma y sujetos sin sensaciones fantasma. Los resultados indicaron que en pacientes que experimentaban el miembro fantasma (con o sin dolor) existía una relación positiva entre el nivel de conductancia de la piel en el muñón y la intensidad de las sensaciones no dolorosas en el miembro fantasma. Asimismo, se encontró una temperatura más reducida en el muñón que en el brazo sano; sin embargo, en sujetos que no tenían la experiencia del miembro fantasma no se encontró ninguna diferencia. Estos resultados sugieren que la percepción del miembro fantasma estaría relacionada con un mecanismo del sistema nervioso simpático que produce vasoconstricción en el muñón. En resumen, el estudio de factores periféricos pone de relieve que el dolor del miembro fantasma no constituye un síndrome unitario sino que se trata más bien de un conjunto de síntomas con diferentes mecanismos etiológicos.
Sin embargo, no cabe duda que la percepción del dolor exige la participación de estructuras corticales. Dos fenómenos perceptuales que aparecen en gran número de amputados apoyan claramente la existencia de mecanismos centrales en la formación del miembro fantasma. Aproximadamente un tercio de los pacientes amputados experimentan una sensación telescópica del miembro fantasma (Weiss y Fishman, 1963; Katz, 1992; Jensen y Rasmussen, 1994; Montoya et al, 1997a). Este fenómeno hace referencia a un proceso gradual de retraimiento (constricción, transformación) del miembro fantasma, en el que las partes más distales de la extremidad fantasma (la mano o el pie) son percibidas próximas al muñón, mientras el resto del brazo amputado va desapareciendo gradualmete. Más tarde, el pie o la mano fantasma comienzan tambien a retraerse y llegan incluso a percibirse como partes immersas completamente en el muñón (Guéniot, 1861; Henderson y Smyth 1948). La relación de este fenómeno con el dolor en el miembro fantasma es controvertida. En algunos trabajos clásicos se había formulado la hipótesis de que la experiencia del fenómeno telescopio podría estar inversamente relacionada con el dolor en el miembro fantasma, de tal forma que cuando éste ocurriese, los pacientes no experimentarían dolor en el miembro fantasma (Henderson y Smyth, 1948; Riddoch, 1941; Weiss y Fishman, 1963). En este sentido, en un estudio realizado por Katz y Melzack (1987) para examinar los efectos de la estimulación eléctrica sobre la percepción sensorial en otras zonas corporales distintas a las estimuladas, se informó del caso de un paciente con dolor del miembro fantasma que durante la estimulacion eléctrica experimentó la sensación de telescopio al mismo tiempo que desaparecía el dolor del miembro fantasma. Sin embargo, contrario a esta hipótesis, Poeck (1963) confirmó la presencia de telescopio en 36 de los 40 pacientes amputados con dolor del miembro fantasma que fueron examinados, y, recientemente, Montoya et al (1997a) encontraron que la incidencia del efecto telescopio se distribuía de forma similar entre amputados con y sin dolor del miembro fantasma.
También es conocido que las sensaciones del miembro fantasma pueden ser moduladas por diferentes factores externos (p.ej., tiempo atmosférico, estrés) y/o factores internos (p.ej., atención, cambios de ánimo). Pero igualmente, pueden ser desencadenadas a través de la estimulación directa del muñón (Carlen et al, 1978; Cronholm, 1951; Haber, 1955; James, 1887; Morgenstern, 1964; Pitres, 1897), así como de otras partes corporales más lejanas al lugar de la amputación, como la cara (Cronholm, 1951; Halligan et al, 1993; Katz y Melzack, 1987; Ramachandran et al, 1992). En estudios recientes realizados por Ramachandran y colaboradores (Halligan et al, 1993; Ramachandran et al, 1992) se observó incluso que estas sensaciones referidas al miembro fantasma estaban organizadas topográficamente y eran desencadenadas de forma reliable. Es decir, se encontró que la correspondencia que existía entre los puntos que producían sensaciones en el miembro fantasma y las zonas del miembro fantasma donde el sujeto percibía esta sensación estaba basada en los mapas corticales que representan el homúnculo somatosensorial. Así se sugería que el hecho de que fueran éstas las zonas corporales desde las que se podían desencadenar las sensaciones fantasmas guardaba estrecha relación con la posición que ocupan dichas áreas en el homúnculo, cercanas a la representación de la mano. A continuación se expondrán los resultados más destacados obtenidos por diversos experimentos llevados a cabo en pacientes amputados. En líneas generales, estos estudios favorecen la hipótesis de que el dolor percibido en el miembro fantasma tras la amputación de una extremidad está relacionado con cambios en la excitabilidad del sistema nervioso central.
III. EFECTOS DE LA AMPUTACIÓN DE UNA EXTREMIDAD SOBRE LA CORTEZA SOMATOSENSORIAL
Una serie de investigaciones realizadas con animales a finales de los años 80 y principio de los 90 ha revelado que la amputación de una extremidad o su denervación producía significativos cambios plásticos en la corteza somatosensorial. Así, por ejemplo, los experimentos de Pons et al (1991) y Merzenich et al (1983) han demostrado alteraciones en los campos receptivos usando microelectrodos implantados en la corteza somatosensorial primaria (area 3b). En particular, se observó que tras la amputación de un dedo la estimulación tactil de los dedos adyacentes producía una activacion de las neuronas que representaban el dedo amputado. Igualmente existe evidencia de que la alteración de las aferencias sensoriales puede producir cambios a largo plazo en la representación somatotópica tanto a nivel subcortical como cortical (Florence y Kaas, 1995; Jain et al, 1997). El término „reorganización cortical" se acuñó para hacer referencia a este ensachamiento de los mapas sobre la corteza somatosensorial, y surgió la cuestión sobre cuáles serían los correlatos conductuales y perceptivos de esta alteración funcional.
Recientemente y gracias al desarrollo de nuevas técnicas de neuroimagen de la actividad cerebral (electroencefalografía, magnetoencefalografía, imágenes de resonancia magnética), se ha podido trasladar este tipo de investigación a sujetos humanos. En general, se aplica una estimulación tactil no dolorosa de forma repetitiva (entre 1 y 4 estímulos por segundo) sobre la piel de la zona a examinar y se registra la actividad electromagnética producida por la estimulación utilizando la técnica psicofisiológica de los potenciales evocados. Los estudios que aquí se revisan emplearon un gran número de canales estrechamente distribuídos sobre la corteza somatosensorial. Para la localización de las fuentes de actividad cortical se emplearon técnicas de análisis de dipolos con ayuda de la información adicional proporcionada por imágenes anátomicas del cerebro obtenidas con registros de resonancia magnética. La organización del homúnculo somatosensorial obtenida por estos medios está en consonacia con diferentes estudios que emplean registros intracorticales (por ejemplo, Baumgartner, 1993) o los clásicos estudios de Penfield y Rasmussen (1952).
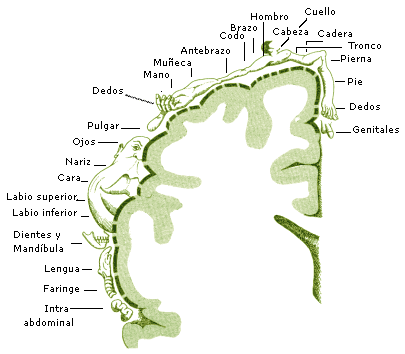
La figura ilustra la representación topográfica de la superficie corporal según el homúnculo somatosensorial (Penfield y Rasmussen, 1952). Como puede verse en la figura, la representación de la mano está limitada en su parte inferior por la cara y en su parte superior por el brazo. Como consecuencia de la amputación de una extremidad superior se ha observado que los mapas corticales correspondientes a la cara (círculo derecho en la figura) y al brazo de la mitad corporal donde se produce la amputación, se extienden hacia la zona ocupada previamente por la mano (cuadrados). Esta alteración de la representación homuncular se denomina reorganización cortical. La intensidad del dolor fantasma que experimentan los pacientes amputados está directamente relacionada con la magnitud de esta alteración.
Ramachandran y colaboradores (Yang et al, 1994) examinaron la hipótesis de que los cambios plásticos ocurridos en la corteza somatosensorial como consecuencia de una amputación podrían explicar la existencia de sensaciones referidas al miembro fantasma cuando se estimula el muñón o el rostro. Esta afirmación aparecía anatómicamente correcta, en cuanto que las representaciones corticales de la cara y el brazo constituyen, respectivamente, las fronteras inferior y superior de la representación de la mano en el homúnculo sensorial. En el estudio, los autores presentaron evidencia de que en un paciente amputado de la extremidad superior derecha aparecían asociados ambos fenómenos. En este paciente, se provocaban sensaciones fantasmas al estimular tanto el brazo derecho como la parte derecha de la cara. Estas regiones aparecían organizadas topográficamente desde la barbilla hasta la mejilla correspondiéndose con los diferentes dedos de la mano fantasma. Igualmente, se encontró un desplazamiento significativo (alrededor de 25 mm) de la localización de la representación cortical de la boca hacia la zona que representaba anteriormente la mano en el hemisferio contralateral a la mitad corporal afectada por la amputación.
En un estudio publicado paralelamente por Elbert et al (1994), se examinó la relación entre reorganización cortical y las sensaciones referidas al miembro fantasma en 5 personas con una amputación unilateral de la extremidad superior. La evaluación de las sensaciones referidas fue realizada según el método de Ramachandran et al (1992). La cantidad de reorganización cortical (es decir, la distancia que la localización que representaba el labio inferior se había desplazado hacia la zona que representaba los dedos de la mano) en la muestra variaba entre 5 y 33 milímetros. Los autores encontraron, sin embargo, que sólo uno de los pacientes presentaba un fenómeno perceptual similar al encontrado por Ramachandran y colaboradores. La cantidad de reorganización cortical obtenida en este paciente, aunque considerable, era superada por otros pacientes que no presentaban este fenómeno perceptivo.
Knecht et al (1996) examinaron sistemáticamente diferentes métodos para producir sensaciones referidas, así como su relación con la reorganización cortical en 8 sujetos con una amputación de la extremidad superior. Para ello se aplicaron 4 modalidades de estimulación (tactil, vibración, temperatura, dolor) sobre la superficie corporal y se recogieron la intensidad y cualidad de las sensaciones experimentadas. De nuevo los resultados no confirmaron la hipótesis formulada por Ramachandran y colaboradores, ya que aunque 7 pacientes experimentaron sensaciones referidas al miembro fantasma tras la estimulación de al menos uno de los métodos empleados, éstas fueron provocadas tanto desde la parte ipsilateral como desde la parte contralateral a la amputación sin guardar ninguna relación topográfica con el homúnculo sensorial. Curiosamente, uno de los resultados significativos de este estudio fue la relación positiva encontrada entre el número de regiones desde la que se producían sensaciones fantasma por medio de la estimulación dolorosa y la cantidad de reorganización cortical. Es decir, la estimulación dolorosa producía un mayor número de sensaciones fantasmas en pacientes que mostraban reorganización cortical, y viceversa.
Así, con excepción del estudio de caso único aportado por Yang et al (1994), los trabajos revisados hasta aquí no han encontrado evidencia empírica que favorezca la atractiva hipótesis de una relación estrecha entre un fenómeno perceptivo relacionado con el miembro fantasma y un proceso fisiológico de alteración plástica de la corteza somatosensorial. Además estos trabajos han demostrado que la generación de sensaciones en el miembro fantasma a través de la estimulación de regiones que ocupan un lugar adyacente a la representación del miembro amputado constituye un fenómeno raro y aislado.
IV. DOLOR DEL MIEMBRO FANTASMA Y REORGANIZACIÓN CORTICAL
A pesar de ello, la idea de que los cambios en la organización funcional del homúnculo observada como consecuencia de una denervación podría tener un correlato „psicológico" no fue abandonada. Así por ejemplo, para Katz (1992) el ensanchamiento de los mapas corticales correspondientes a áreas vecinas a la zona amputada podría constituir el correlato fisiológico del fenómeno telescopio observado en algunos pacientes amputados. Asimismo, se sugirió que este proceso fisiológico podría tener una función adaptativa para el sujeto al reducir el dolor en el miembro fantasma.
Partiendo de esta hipótesis, Flor et al (1995) examinaron la relación existente entre la presencia de dolor del miembro fantasma y la reorganización cortical en una muestra de 13 pacientes con amputación unilateral de la extremidad superior. Para ello se llevó a cabo la localización de los mapas corticales somatosensoriales de manera similar a la descrita anteriormente y se realizó una entrevista detallada y semiestandarizada sobre diferentes fenómenos asociados con la amputación, incluyendo el dolor fantasma actual e immediatamente posterior a la amputación, las sensaciones fantasmas no dolorosas y el dolor en el muñón (para una descripción del instrumento de evaluación, véase también Montoya et al, 1997a). No se confirmó ninguna relación significativa entre la cantidad de reorganización cortical y la mayoría de las variables examinadas (telescoping, otros fenómenos no dolorosos del miembro fantasma, intensidad del dolor en el muñón, tiempo transcurrido desde la amputación). Sin embargo, los autores encontraron una correlación positiva y altamente significativa (r = 0.93) entre el dolor en el miembro fantasma y la cantidad de reorganización cortical. Así, la hipótesis y sugerencia formulada por Katz (1992) de que los cambios plásticos de la corteza somatosensorial podrían constituir un mecanismo compensatorio al restablecer la función en un área deprivada de aferencias nerviosas, no pudo ser confirmada. Por el contrario, los resultados apuntaban hacia una función maladaptativa de la plasticidad cortical en pacientes amputados con dolor en el miembro fantasma. Como posible mecanismo fisiológico se postuló que un estado permanente de hiperexcitabilidad cortical producido por un desequilibrio entre las vías nociceptivas y no-nociceptivas incluso antes de la amputación podría ser responsable de mantener esta relación. Conforme a esta hipótesis, el estudio de Knecht et al (1996) sugiere también que la relación observada entre la producción de sensaciones fantasmas por medio de estimulación dolorosa y la reorganización cortical podría estar modulada por la influencia de aferencias nociceptivas.
Montoya et al. (1997) analizaron los mapas corticales en 5 sujetos con una amputación por traumatismo de una extremidad superior y con dolor en el miembro fantasma, así como en 4 personas con malformaciones de la extremidad superior desde el nacimiento y 5 personas sanas. El objetivo del estudio era doble: en primer lugar, se examinó si la deprivación sensorial en las fases tempranas del desarrollo de una extremidad producía los mismos cambios plásticos funcionales que los observados en pacientes amputados; en segundo lugar, se realizó un análisis más completo de la organización homuncular de la corteza somatosensorial al obtener el mapa cortical correspondiente a la representación del pie. La evidencia procedente de estudios con animales sugiere que la formación de los mapas corticales y subcorticales se puede alterar si se daña la extremidad durante el período prenatal (Killackey et al, 1995; Rhoades et al, 1994). Asimismo, se ha hipotetizado que estos efectos son diferentes a los producidos en la etapa postnatal (Kandel y O'Dell, 1992). Sin embargo, no estaba claro hasta qué punto era posible trasladar estos resultados a sujetos humanos con un período de maduración fisiológica diferente al de los animales de experimentación. El presente estudio confirmó nuevamente los resultados previos obtenidos por Flor et al (1995), al mostrar una alteración funcional de la corteza somatosensorial sólo en pacientes con dolor en el miembro fantasma. Además se encontró que dichas alteraciones afectaban exclusivamente a la representación cortical de la cara y no a la extremidad inferior. Es decir, se demostró que la plasticidad asociada con el dolor en el miembro fantasma se limita a los mapas adyacentes a la representación cortical del miembro amputado. Asimismo se observó que el mapa cortical de los sujetos con malformaciones desde el nacimiento no se diferenciaba del obtenido en sujetos sanos. Estos resultados favorecen la hipótesis de que la reorganización cortical en pacientes amputados está estrechamente relacionada con la experiencia del dolor en el miembro fantasma.
Una vez visto que el ambos fenómenos parecen estar en relación directa, el siguiente paso sería la evaluación de hasta qué punto se trata de un fenómeno cortical mantenido por el input procedente de la periferia o es independiente de éste. Un método adecuado para examinar la implicación de estos niveles en el procesamiento del dolor lo proporciona el uso de la anestesia regional o local. Así, el bloqueo del plexo axilar en la zona de la extremidad superior o el bloqueo de los nervios principales que innervan la extremidad inferior (ischiadicus, femoralis y obturatorius) puede servir para analizar los efectos que la paralización de la información a estos niveles produce sobre el dolor del miembro fantasma y sobre los cambios plásticos de la corteza somatosensorial.
Este fue el objetivo del estudio publicado recientemente por Birbaumer et al (1997). La reorganización cortical fue examinada en 10 pacientes con una amputación unilateral de la extremidad superior durante una línea base y bajo los efectos del bloqueo sensomotor del muñón y resto del brazo. La anestesia regional se llevó a cabo usando la técnica del bloqueo del plexo braquial a nivel infraclavicular con 30-40 ml de Mepivacaína al 2% mezclado con una solución de adrenalina (1:200000). Según la entrevista realizada previamente, 6 pacientes sufrían de dolor crónico en el miembro fantasma y 4 pacientes no tenían ningún tipo de sensaciones dolorosas. Los datos de la línea base confirman una mayor reorganización cortical en pacientes con dolor (20 mm) que en pacientes sin dolor (3 mm). Como consecuencia de la anestesia, 3 pacientes con dolor en el miembro fantasma experimentaron una reducción significativa del dolor (de 4.2 pasó a 0.4 en una escala numérica con 0 = no dolor y 6 = máximo dolor). En los 3 sujetos restantes, el dolor permaneció a pesar del bloqueo (línea base = 5.1, post-anestesia = 5.1). En los sujetos que no sufrían previamente de dolor la anestesia no produjo ningún cambio en la percepción del miembro fantasma. Los resultados sobre la reorganización cortical fueron similares a los obtenidos sobre el dolor. Los pacientes que experimentaron una reducción del dolor redujeron tambien la reorganización cortical. Es decir, la localización de la representación cortical de la boca sobre el hemisferio que procesaba la parte amputada se había desplazado hacia una posición más simétrica con respecto a la del hemisferio opuesto. Esta nueva reorganización funcional de la corteza somatosensorial como consecuencia de la anestesia regional fue aproximadamente de 18 mm. Aquellos sujetos en los que la anestesia no produjo un efecto significativo la reorganización cortical fue apenas modificada (2 mm). Los resultados de este estudio muestran una relación positiva entre la reducción del dolor en el miembro fantasma y la reducción de la reorganización cortical, sugiriendo una relación funcional entre ambos fenómenos. La estrecha asociación entre la reducción de las aferencias sensoriales, eliminación del dolor y modificación de la reorganización cortical en un grupo de pacientes amputados está de acuerdo con la idea de que los dolores en el miembro fantasma resultante de una denervación son el producto del predominio de las aferencias nociceptivas sobre las no-nociceptivas. Asimismo, es bastante probable que los rápidos cambios plásticos producidos por el bloqueo sensorial a través de la anestesia haya sido debido a una desinhibición de conexiones talamo-corticales y cortico-corticales que normalmente ejercen una influencia inhibitoria (Rausell et al, 1992). Los cambios plásticos de la corteza somatosensorial que permanecen a pesar del bloqueo de las aferencias periféricas están probablemente relacionados con conexiones sinápticas basadas en procesos de regeneración axonal o de aprendizaje neuronal de acuerdo a las leyes de Hebb (Darian-Smith y Gilbert, 1994; Diamond et al, 1994). Asimismo, se sugirió que estas modificaciones plásticas tan resistentes podrían ser la causa de la ineficacia de muchos tratamientos contra el dolor en el miembro fantasma dirigidos exclusivamente a actuar sobre los mecanismos periféricos aferentes.
V. MECANISMOS FISIOLÓGICOS DEL DOLOR EN EL MIEMBRO FANTASMA
Desde el punto de vista fisiológico, el dolor crónico refleja un exceso de excitabilidad del sistema somatosensorial (Woolf y Doubell, 1994). Esta sensibilidad anormal es básicamente el producto de una alteración en el funcionamiento del sistema nervioso central como respuesta a una patología producida en la periferia. La hiperexcitabilidad asociada al dolor puede ocurrir en cuestión de minutos tanto por una reducción del umbral de los nociceptores en el lugar de la lesión como por un aumento en la responsividad de las neuronas espinales. En el caso de los síndromes de dolor por denervación sensorial (dolor en el miembro fantasma, anestesia dolorosa, y lesión del plexo braquial), el dolor es claramente independiente de la información que llega de la periferia hacia el sistema nervioso central. Los resultados descritos aquí sugieren que en pacientes amputados el aumento de excitabilidad que genera el dolor en el miembro fantasma se refleja en cambios plásticos de la corteza somatosensorial. Pero, ¿cuáles son los mecanismos fisiológicos responsables de este aumento de la excitabilidad neuronal? El corte de las aferencias nerviosas que causa la amputación de una extremidad produce una serie de cambios anatómicos y fisiológicos que afectan no sólo a los axones de las neuronas sensoriales primarias, sino también a partes alejadas de éstas, como los cuerpos celulares y las sinapsis en la espina dorsal. Es conocido que la transmisión nerviosa de las sensaciones somáticas se produce fundamentalmente por medio de fibras A-beta, A-delta y C. En un estado normal del organismo, las primeras responden ante estímulos de baja intensidad y producen una sensación no dolorosa. Se trata de fibras mielinizadas asociadas con mecanoreceptores altamente especializados de la periferia. Las fibras A-delta y C responden ante estímulos de alta intensidad y su activación genera una sensación dolorosa. Se ha hipotetizado que en un estado de dolor crónico se produce probablemente un cambio en la excitabilidad de las fibras A-beta, originando dolor ante estímulos de baja intensidad (Treede, 1992; Woolf y Doubell, 1994). Según estos modelos existen, al menos, 3 mecanismos que intervienen en esta modificación de la sensibilidad de las fibras A-beta a nivel de la espina dorsal. Así, por ejemplo, un aumento de la excitabilidad en las neuronas aferentes nociceptivas como las fibras C podría provocar una disminución del umbral de excitación de las fibras A-beta en el asta dorsal de la médula espinal que condujera a producir alteraciones en el sistema de procesamiento central. Pero también una disminución de neurotransmisores en las interneuronas que modulan la actividad de las fibras A-beta provocaría un aumento de la actividad de estas fibras y la generación de dolor. Por último, la participación de las fibras A-beta en la transmisión nociceptiva pueder ser la consecuencia de un proceso de reorganización estructural en el asta dorsal de la médula espinal como ha sido puesto de relieve en algunos experimentos con animales (Woolf y Doubell, 1994) y casos clínicos (Baron y Saguer, 1993).
Existen indicios de que esta hiperexcitabilidad de las fibras A-beta pudiera ser también responsable del dolor en el miembro fantasma. Baron y Maier (1995) examinaron un paciente con amputación de la pierna derecha y una lesión unilateral (parte izquierda) del sistema nociceptivo central a nivel de la médula oblongada encargado, principalmente, de transmitir la información de fibras A-delta y C. A pesar de la falta completa de sensibilidad para el dolor en la mitad derecha del cuerpo, el paciente experimentaba dolor en el pie fantasma (derecho). Además la estimulación del muñón por medio de una corriente eléctrica aplicada sobre la piel aumentaba el dolor fantasma. Debido a la lesión en el sistema nociceptivo central, es bastante improbable que el dolor estuviera modulado por aferencias nociceptivas. Por tanto, este estudio favorece la hipótesis de un exceso de excitabilidad de las fibras A-beta en el mantenimiento del dolor en el miembro fantasma.
VI. CONCLUSIONES
En primer lugar, los estudios descritos en esta revisión demuestran que la representación homuncular de la superficie corporal en la corteza somatosensorial está sujeta a modificaciones funcionales cuando se cortan las aferencias nerviosas que transmiten la información somatosensorial desde la periferia. Este fenómeno, extensamente estudiado en animales, ha sido extendido a sujetos humanos gracias a la posibilidad de obtener mapas funcionales de la corteza somatosensorial por medio de técnicas de imágenes cerebrales no invasivas. De forma paralela a los estudios con animales, se ha encontrado una alteración significativa de los mapas corticales de zonas corporales adyacentes a la extremidad amputada en sujetos amputados de la extremidad superior. Estas alteraciones afectan sólo a los mapas corticales sobre el hemisferio encargado de procesar la información somatosensorial procedente de la mitad corporal correspondiente a la amputación. Asimismo, se ha demostrado que estas alteraciones son más extensas en sujetos que padecen de dolor en el miembro fantasma que en amputados sin dolor. Aunque estos cambios plásticos han sido observados en la corteza cerebral, no es descartable que éstos sólo sean el reflejo de alteraciones producidas a nivel subcortical. Además cabe subrayar que estos estudios apuntan claramente hacia una interacción entre mecanismos centrales y periféricos en el mantenimiento y, probablemente, el origen de los dolores en el miembro fantasma que siguen a la amputación de una extremidad. A pesar de que los estudios realizados hasta la fecha examinan a pacientes con una amputación de la extremidad superior, no existen razones fundadas pare pensar que dichos fenómenos no ocurran también en pacientes tras la amputación de la extremidad inferior.
Las implicaciones clínicas para el tratamiento del dolor en el miembro fantasma son evidentes: deben desarrollarse terapias que dirijan su objetivo principal a modificar la alteración de los mapas corticales que se presentan en los pacientes amputados. Así cualquier tipo de medida que implique un reaprendizaje de la organización funcional del homúnculo sensorial debe producir indirectamente un alivio del dolor en el miembro fantasma. Aunque aún faltan estudios que demuestren la exactitud de esta hipótesis, recientes estudios sobre aprendizaje y plasticidad cortical ya han demostrado que la organización de la corteza somatosensorial también es modificable por medio del aprendizaje en sujetos sanos (Jenkins et al, 1990).
Por último, hay que señalar el papel relevante que juega la terapia de prevención del dolor en el caso de los amputados. Teniendo en cuenta que entre el 50 y el 90% de los amputados experimentan los primeros dolores en el miembro fantasma alrededor de una semana tras la amputación (Jensen y Rasmussen, 1994), no cabe duda que las medidas encaminadas a reducir los mecanismos periféricos nociceptivos que desemboquen en cambios plásticos duraderos deben ser tomadas desde el primer momento. Una confirmación de la aplicación eficaz de tales medidas fue encontrada por Bach et al (1988) al demostrar que sujetos que habían sido mantenidos sin dolor durante tres días consecutivos previos a la amputación habían desarrollado posteriormente menos dolor que pacientes tratados de forma estándar. Sin embargo, pruebas primordialmente basadas en estudios prospectivos han de aclarar el papel que juegan este tipo de medidas en el caso del dolor en el miembro fantasma y la reorganización cortical.
VII. NOTAS
(1) El cirujano del ejército francés Ambroise Paré (1510-1590) describe el dolor en el miembro fantasma por primera vez en 1531. ==========================================================================
PEDRO MONTOYA
UNIVERSIDAD DE LAS ISLAS BALEARES
Dirección para correspondencia:
Dr. Pedro Montoya
Departamento de Psicología Básica - Universidad de las Islas Baleares
Carretera de Valdemossa, km. 7,5
E-07071 - Palma de Mallorca
Islas Baleares - SPAIN




